Бактерии рода Streptomyces sp.- основа препарата Веривер
16 января 2025, 23:07
журнал Гавриш №2
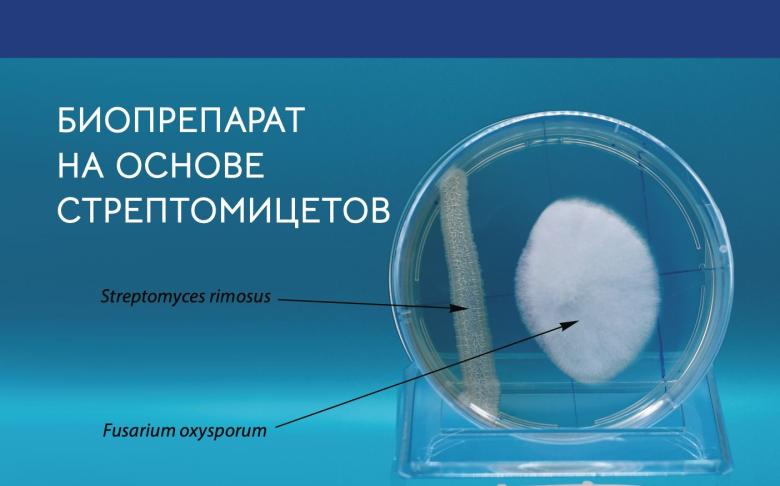
В статье проведено исследование различных свойств бактерий рода Streptomyces spp, для оценки перспективности использования данных бактерий в качестве агентов биологического контроля. Проведена оценка фитотоксичности различных штаммов бактерий рода Streptomyces spp по отношению к огурцам гибрида F1 Атлет и томатам гибрида F1 Сумо. Оценены бактерицидные и фунгицидные штаммов бактерий рода Streptomyces spp. Исследована способность метоболизма экссудатов растений и колонизации корневой системы растений.
В результате данного исследования показана перспективность использования бактерий рода Streptomyces spp в качестве агента биологического контроля, при создании биологических препаратов для использования в системах защиты растений, выращиваемых в защищенном грунте.
Формирование микробного сообщества
Одной из первостепенных задач биологической защиты, при выращивании растений в защищенном грунте, с применением в качестве субстрата для выращивания-минеральной ваты (или аналогичных инертных субстратов), является наискорейшее управляемое формирование микробного сообщества в прикорневой зоне растения. Причем, для формирования микробного сообщества необходимо использовать фитоположительную микрофлору. В дальнейшем микробное сообщество необходимо постоянно корректировать в соответствии с теми технологическими решениями, которые используют агротехнические службы комбината, и в соответствии с фазой развития растений.
Первостепенность формирования микробного сообщества обусловлена следующим фактором - минераловатный субстрат после его производства не содержит в своем составе микроорганизмов, он практически стерилен, но как только происходит напитка поливными растворами, в субстрат попадают разные группы микроорганизмов в том числе фитопатогенные. После посева семян или посадки растений в минеральную вату начинают выделяться органические компоненты - экссудаты, выделяемые растениями через корневую систему [1]. Количество выделяемых органических компонентов пропорционально росту растения и эти выделения состоят из моно- и ди- сахаров, органических кислот цикла Кребса, небольшого количества различных аминокислот [2]. Текущая концентрация органических соединений в прикорневой зоне растения зависит от скорости их выделения и скорости потребления теми микроорганизмами, которые находятся в этот момент в прикорневой зоне и на поверхности самих корней. Наши исследования показали, что в прикорневой зоне концентрация экссудатов колеблется от 20 до 200 мг/л в пересчете на глюкозу [2]. Данные концентрации являются для многих микроорганизмов лимитирующими их рост и при них многие микроорганизмы растут со скоростями много ниже, чем максимальные скорости характерные для данных условий [2]. Фитоотрицательные микроорганизмы, в результате длительной эволюции, приобрели способность к росту с максимальной скоростью при минимальных остаточных концентрациях экссудатов [3]. Для снижения вероятности развития фитоотрицательной микрофлоры в прикорневой зоне и необходимо управляемое формирования микробного ценоза с использованием фитоположительной микрофлоры. Формирование микробного сообщества и последующее его регулирование позволяет резко снизить использование химических препаратов, в том числе обладающих системными свойствами и перейти к понятию - экопочва.
Наши многолетние исследования микробного сообщества прикорневой зоны томатов и огурцов на разных стадиях развития, на минераловатных субстратах различных производителей позволили нам сделать предположение, что микробный биом минераловатного субстрата в своей основе приближается по концентрации микроорганизмов к микробному биому различных почв и составляет порядка 109 КОЕ/г (не опубликованные данные). Видовой состав биоты, в минераловатной почве зависит от массы факторов, и в первую очередь, от той микрофлоры, которая вносится в него с биологическими препаратами, с потоками воды, оседает из воздуха. Распределение микроорганизмов по глубине также зависит от массы факторов – влажности, насыщенности поливного раствора, растворенным кислородом, да и самой структурой минеральной ваты. Соотношение бактериальной и грибной микрофлоры в минеральной вате приближается к 109 КОЕ/г бактерий и 105 КОЕ/г грибов [4,[5]]. Среди бактерий распределение на Г+ и Г- приблизительно одинаковое. Бактерии представлены достаточно широким родовым и видовым разнообразием, но в минераловатном субстрате при развитии в нем корневой системы разных растений мы крайне редко встречали микроорганизмы - представителей рода Streptomyces spp. В природных почвах, по данным различных авторов [6] в почвах различных типов бактерии рода Streptomyces spp составляют достаточно большой процент, и их концентрация может доходит до 107 КОЕ/г [7]. Отсутствие бактерий рода Streptomyces spp в минераловатном субстрате связано с физиологией развития, как самих бактерий рода Streptomyces spp, так и с тем, что за ограниченный период времени выращивания растений эти микроорганизмы не успевают в достаточной мере колонизировать минераловатный субстрат.
Бактерии рода Streptomyces spp
Бактерии рода Streptomyces spp. являются почвенными аэробными микроорганизмами, в состав рода которых входит порядка 688 видов [8] и судя по свойствам, которые они проявляют при взаимодействии с микроорганизмами ризосферы [10], являются перспективными объектами для применения в технологии биологической защиты растений. Перспективность и применения бактерии рода Streptomyces spp. обусловлена физиологией их роста - они способны к мицелиальному росту [8], причем апикальный рост мицелия и его ветвление происходит в сторону наиболее благоприятную для этого, что в условиях пониженных концентраций доступных органических компонентов питания, что позволяет бактериям рода Streptomyces spp более полно, чем остальным микроорганизмам заполнять физиологически активную поверхность субстрата. При делении бактерий рода Streptomyces spp выделяют большое количество разнообразных биологически активных соединений бактерицидного и фунгицидного действий [9,10], данный факт указывает на то, что возможно снижение в субстрате уровня концентрации фитоотрицательной микрофлоры различной природы.
На первом этапе исследования проводили выбор штаммов, перспективных для создания биологических средств защиты растений. Была определена способность штаммов бактерий рода Streptomyces spp. метаболизировать экссудаты корневой системы огурцов и томатов. При тех концентрациях, которые устанавливаться в прикорневой зоне растений.
Все проверенные нами штаммы показали способность к росту на агаризованных средах, где единственными источниками углерода были экссудаты корневых выделений или огурца, или томата.
Среди представителей бактерий рода Streptomyces spp встречаются виды, вызывающие заболевания растений, в частности парша картофеля, поэтому следующим этапом скренинга штаммов проводили на их фитотоксичность.
Исследования штаммов
Для исследования фитотоксичности в чашку Петри с 2 слоями стерильной фильтровальной бумаги (марка Ф) увлажняли его 3 мл стерильной воды (контроль) или 3 мл. разбавленной культуральной жидкостью, исследуемого штамма. В полученные влажные камеры высаживали семена огурца гибрида F1 Атлет или семена томата гибрида F1 Сумо. Все варианты исследовали в нескольких повторностях. Проращивали семена в течение 7 суток в одинаковых условиях в термостате при температуре 28°С, без освещения. На 3 сутки определяли энергию прорастания семян, на 7 сутки - всхожесть согласно ГОСТ [11]. Также на 7 сутки определяли среднюю длину корневой системы, среднюю длину вегетативной части проростков, среднюю массу проростков.
После измерения всех параметров оценивали фитотоксичный эффект [12] по формуле:
где Mк – средняя масса проростков в контрольной пробе
Моп – средняя масса проростков в опытной пробе
В случае, если показатель фитотоксичности больше 15%, то образец считался токсичным для растений, если менее -15%, то фитостимулирующим. В случае, если фитотоксичный эффект попадает в интервал от -15% до 15%, то эффект образца нейтрален.
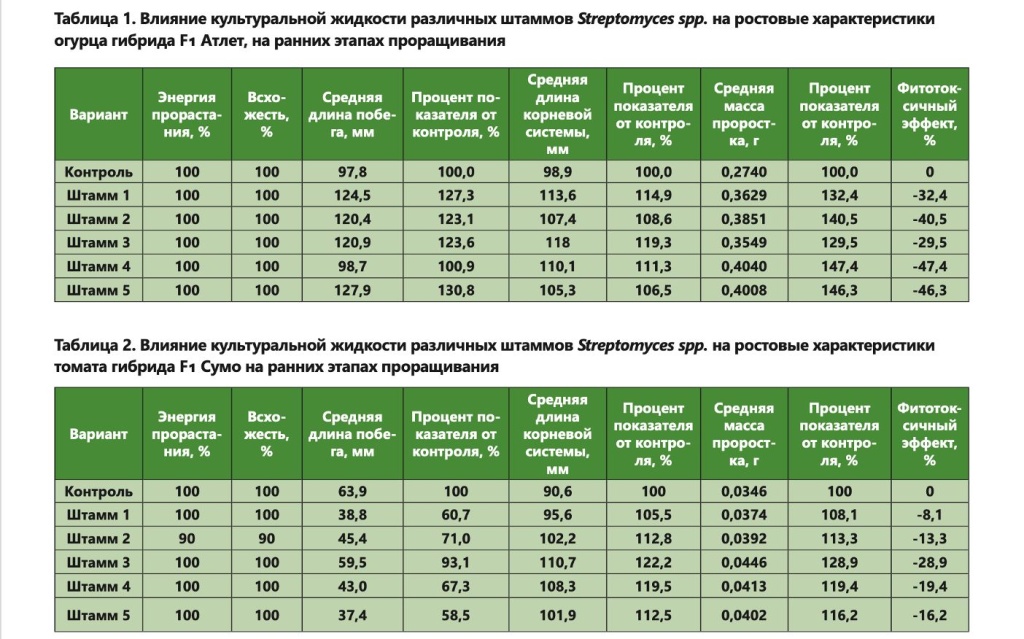
Большинство исследованных штаммов проявили эффект фитостимулирования. Об этом свидетельствовали данные по увеличению средней длинны корневой системы и в целом массы проростков.
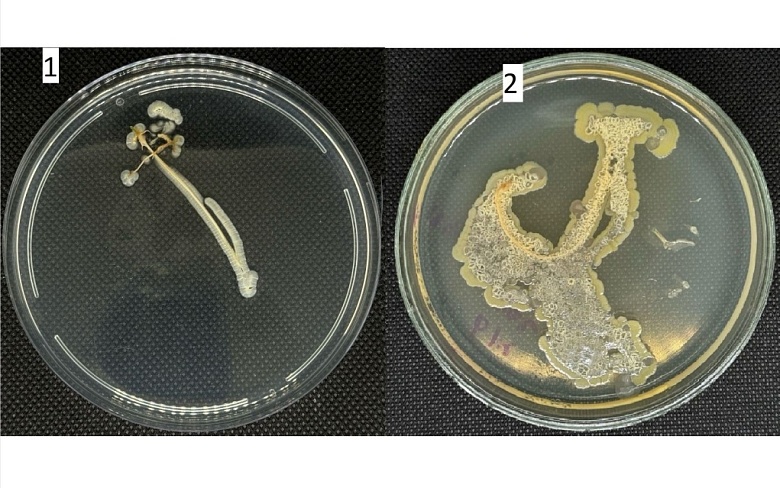
Очень важным свойством фитоположительных микроорганизмов является способность их к сорбции на корневой системе и её колонизации и тем самым препятствование сорбции фитопатогенных микроорганизмов, Исследуемые нами штаммы бактерий рода Streptomyces spp. были проверены на способность клеток сорбироваться на поверхности корневой системы огурцов и томатов. На рисунке 1 показаны корневые системы растений, выращенные в присутствии исследуемых клеток и выложенные в дальнейшем на агаризованные среды, после чего определена принадлежность микроорганизмов на поверхности корневых систем к бактериям рода Streptomyces sp.
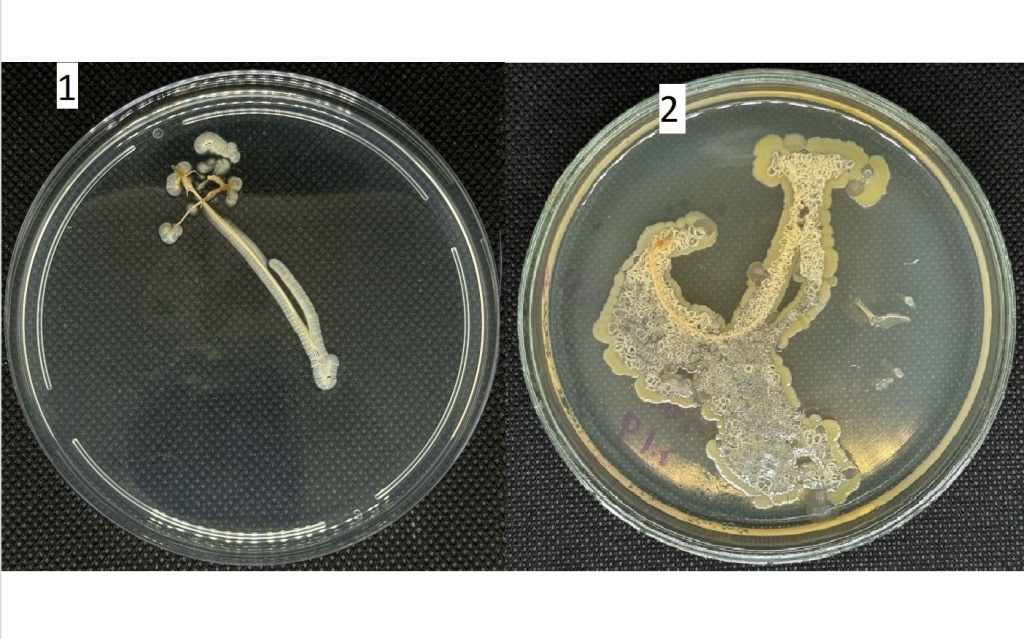
Рисунок 1 – Развитие бактерий рода Streptomyces spp. на поверхности корневой системы томата (1) и огурца (2).
Как видно из рисунка 1 корневая система растения полностью покрыта клетками исследуемых штаммов. Таким образом, было подтверждено, что клетки исследуемых штаммов достаточно хорошо сорбируются на поверхности корневой системы. Десорбция клеток с поверхности корневой системы в стерильные растворы аналогичные тем, в которых выращивали растения, показала, что часть клеток десорбируется, при этом бактерии рода Streptomyces spp были обнаружены и на поверхности корней, с которых проводили десорбцию. Это подтверждает то, что клетки образуют на поверхности корневой системы достаточно устойчивые биопленки.
Бактерии рода Streptomyces spp, являясь почвенными микроорганизмами, в процессе эволюции приобрели способность к синтезу биологически активных соединений [13] антибиотического характера к представителям разных групп микроорганизмов ризосферы и одновременно со способностью клеток к росту на экссудатах корневой системы растений это делает их перспективными объектами для регулирования численности фитопатогенной грибной и бактериальной микрофлоры в прикорневой зоне растений.
Взаимодействие бактерии рода Streptomyces spp и фитопатогенной микрофлоры оценивали по стандартной консервативной методике, методом «лунок» [14], как на стандартах агаризованных средах, так и на средах содержащих модель экссудатов при достаточно низких концентрациях. В качестве объекта воздействия бактерии рода Streptomyces spp были выбраны бактерии Clavibacter michiganensis subsp. michiganensis (C.michiganensis) возбудителя бактериального рака томата [15] и Rhizobium radiobacter (Agrobacterium tumefaciens)(R. radiobacter) вызывающих разрастание корней [16].
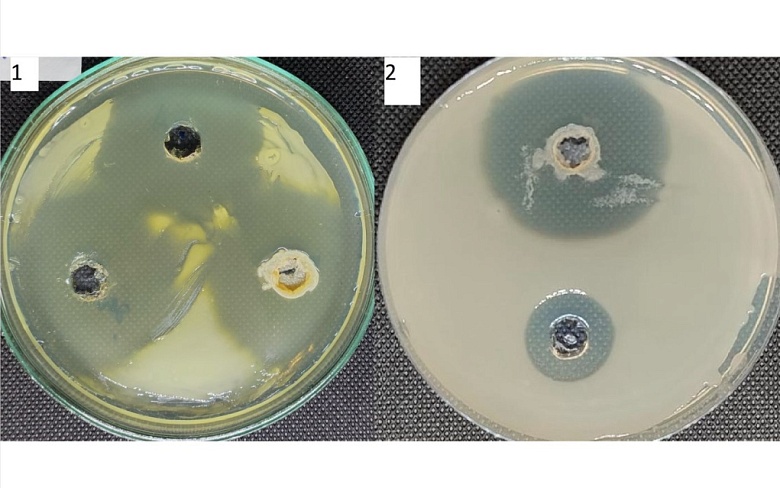
На рисунке 2 представлены результаты культивирования выбранных микроорганизмов на агаризованных средах с лунками, в которые вносили фиксированные растворы суспензии клеток исследуемых штаммов бактерий рода Streptomyces sp.
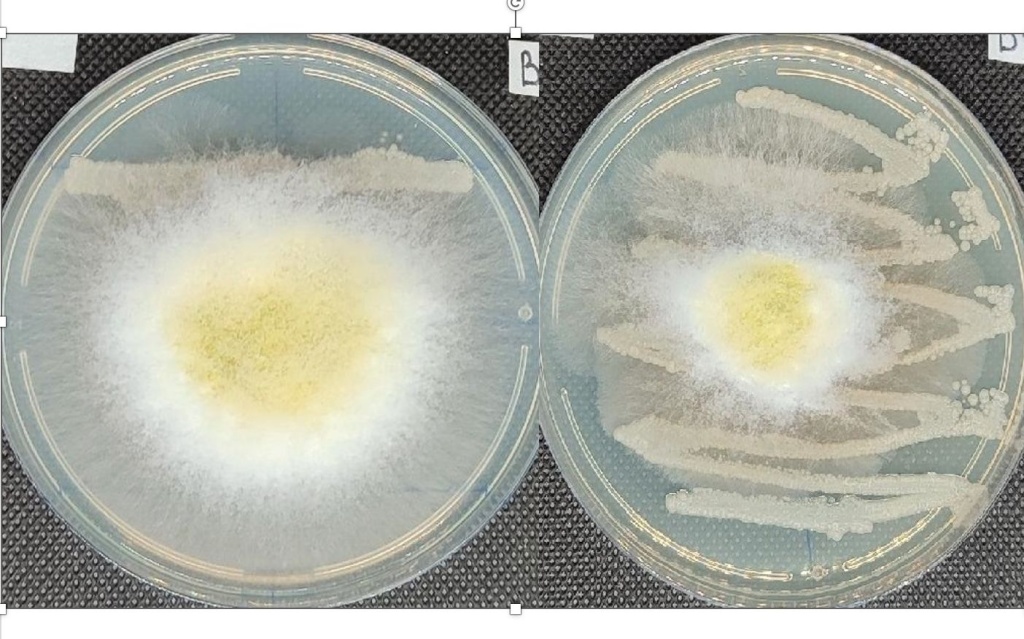
Рисунок 2. Проявление бактерицидных свойств Streptomyces sp по отношению к R. radiobacter (1) и C.michiganensis (2).
Как видно клетки Streptomyces sp подавляют развитие, как бактерий C.michiganensis, так и бактерий R. radiobacter, причем подавление происходит, как культуральной жидкостью не содержащей клетки, так суспензией клеток отмытых от культуральной жидкости. Аналогичные результаты были получены при проведении исследований на агаризованных средах содержащих модель экссудатов в концентрациях, преближенных к концентрациям в ризосфере растений огурца и томата.
Результаты свидетельствует о том, что бактерий рода Streptomyces sp способны к синтезу биологически активных веществ при их росте на модельных системах, содержащих экссудаты корневой системы растения.
Оценку фунгицидных свойств бактерий Streptomyces spp проводили следующим образом. В чашке Петри на поверхность агаризованной среды (Чапек и МЭ) в центр уколом подсевали тест-объект (Fusarium oxysporum, Alternaria sp., Botrytis sp.), затем, отступая 1,5-2 см от центра при помощи микробиологической петли проводили штрих биомассой Streptomyces sp. В качестве контроля выступала сторона чашки, на которой не было штриха. Далее чашки Петри помещали в термостат для инкубации при температуре 28 °С в течение 72 часов. По окончании инкубации сравнивали радиус грибной колонии на контрольной стороне и на стороне со штрихом Streptomyces spp..
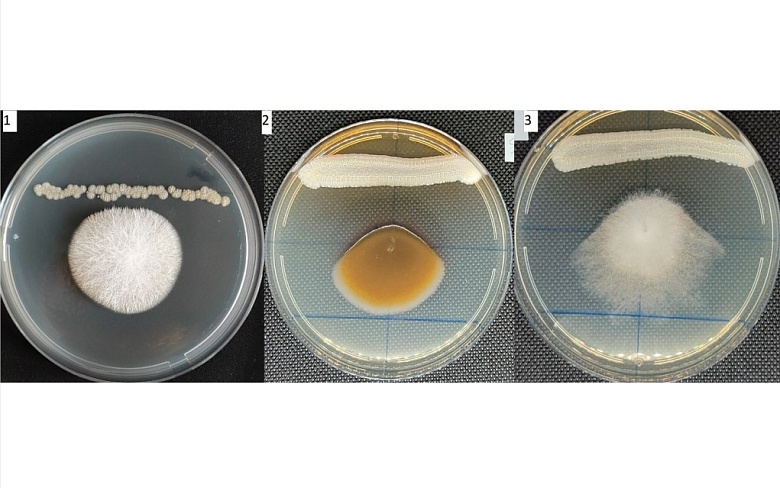
На рис 3 представлены результаты экспериментов по исследованию воздействия бактерии рода Streptomyces spp фитопатогенные грибы.
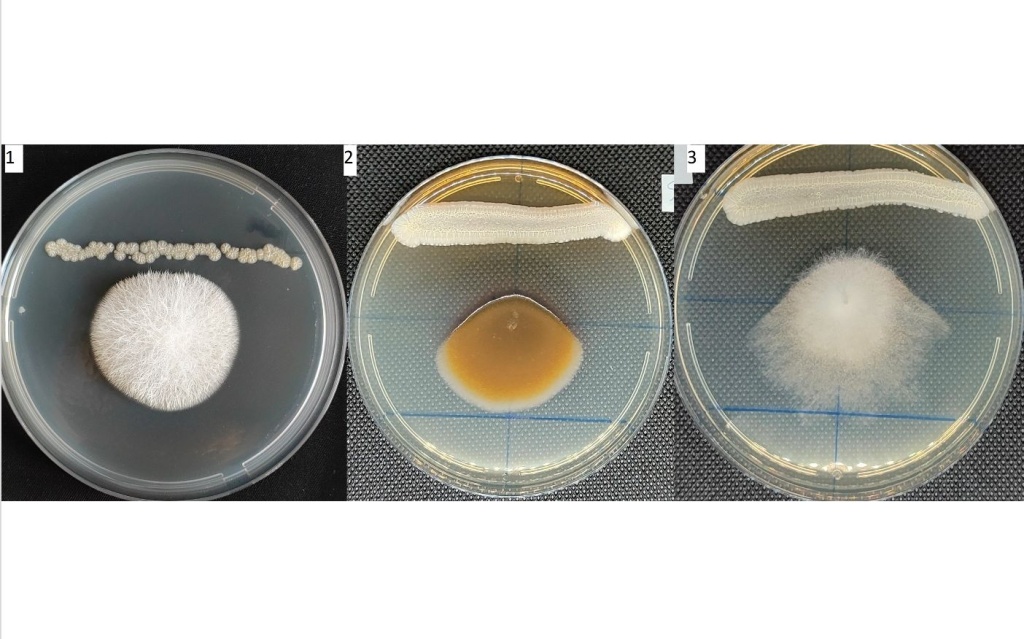
Рисунок 3. Фунгицидные свойства бактерий рода Streptomyces spp по отношениям к грибам рода Fusarium sp. (1), Alternaria sp (2), Botritis sp. (3).
Во всех случаях наблюдалось подавление роста тест объектов бактериями рода Streptomyces spp. При проверке бактерий Streptomyces spp на рост фитопатогенных грибов на агаризованных средах с экссудатами при концентрациях, приближенным к концентрациям в ризосфере, по методике, когда биомасса бактерий Streptomyces spp наносились штрихом, а исследуемый гриб наносился в центр агаризованной среды уколом , как показано на рисунке 3, было обнаружено, что развитие фитопатогенных грибов имеет преимущественное развитие от места, где растут бактерии Streptomyces spp, Это явление, направленного роста грибов в сторону наиболее благоприятную для них, еще раз подтверждает, что бактерии Streptomyces spp являются перспективным объектом для разработки препаратов биологического контроля.
Одновременно с фитопатогенными микроорганизмами в прикорневой зоне растения развиваются и фитоположительные микроорганизмы, в том числе те, которые специально вносят в ризосферу при формировании микробного ценоза. К таким микроорганизмам относятся грибы рода Trichoderma spp., широко используемые как фитоположительные микроорганизмы. Важным было подобрать штаммы бактерий Streptomyces spp, воздействие которых было бы минимально на грибы рода Trichoderma spp., используемыx в препаратах для биологического контроля.
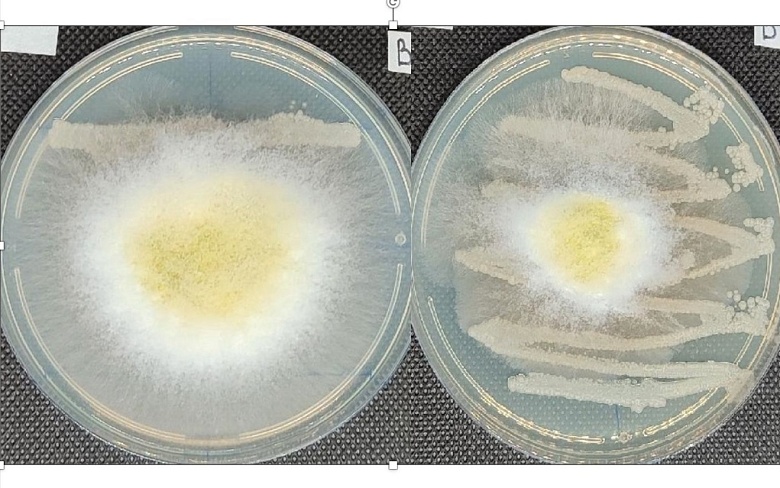
Исследования, проведенные нами, по изучению взаимодействия грибов рода Trichoderma sp. и разных штаммов бактерий рода Streptomyces spp, позволили выделить штамм (рисунок 4), который при сохранении всех своих положительных свойств – способности к метаболизму экссудатов, сорбции на корневой системе растения, проявлении бактерицидных и фунгицидных свойств по отношению к фитоотрицательной микрофлоре, не подавляет развитие грибов рода Trichoderma spp.
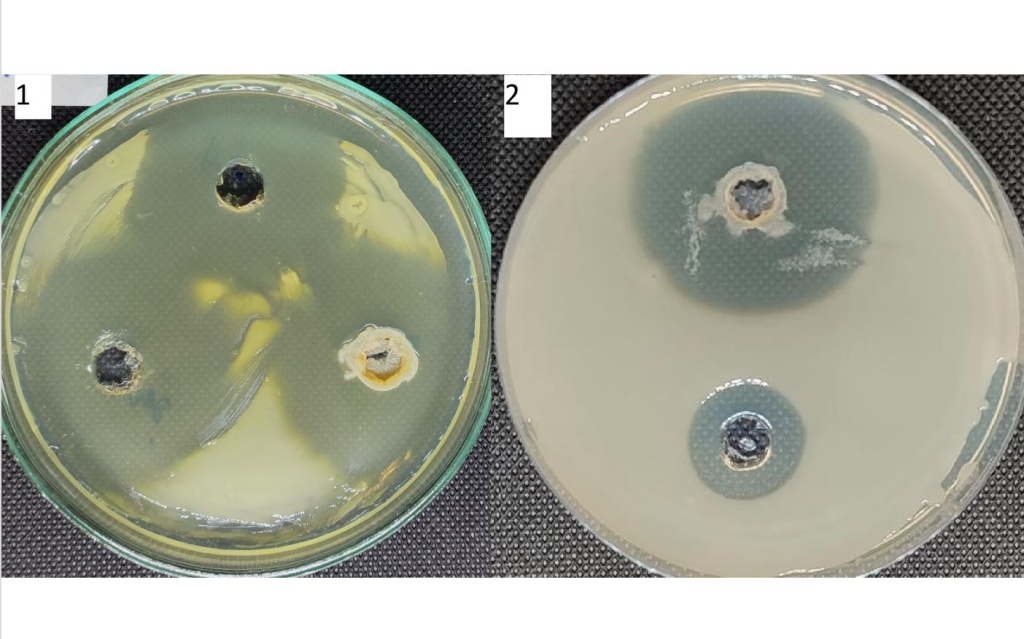
Рисунок 4 – Отсутсвие проявления фунгицидных свойств, выбранного штамма Streptomyces sp., по отношению к грибу Trichoderma sp.
Результаты исследований получены как на стандартных агаризованных средах, так и при проведении испытаний на среде, моделирующей экссудаты огурца и томата при концентрациях, приближенным к концентрациям в ризосфере растений
.Таким образом бактерий рода Streptomyces spp в силу целого комплекса свойств являются перспективным объектом для создания препаратов для биологической защиты растений. Один из штаммов бактерий рода Streptomyces spp был выбран нами, на основе своих свойств, для создания препарата ВЕРИВЕР, Ж (ГК БИОМ), который можно использовать как на стадии формирования микробного сообщества в прикорневой зоне растений, так и на стадиях корректировки его состава для регулирования численности грибных и бактериальных фитопатогенов.
Список используемой литературы
- Д.Г. Титова*, А.Г. Буланов, О.М. Филатова, Е.Н. Дмитриева, О.Б. Горюнова, Н.С. Марквичев, А.А. Белов Роль экссудатов корневой системы огурца в формировании микробного ценоза при выращивании по малообъемной технологии //Успехи в химии и химической технологии. – 2014. – Т. 28. – №. 5 (154). – С. 70-73.
- А. А. Шагаев, А. С. Журавлева, Н. Б.-о. Бехбудзада, Марквичев Н.С. и др. Повышение продуктивности растительных экосистем регулированием уровня фитопатогенеза Fusarium oxysporum экссудатами корневой системы растений // Химическая промышленность сегодня. — 2023. — № 2. — С. 7–12. (CAS)
- Musilova L. et al. Effects of secondary plant metabolites on microbial populations: changes in community structure and metabolic activity in contaminated environments //International journal of molecular sciences. – 2016. – Т. 17. – №. 8. – С. 1205.
- Минеральная вата нового поколения — формирование микробного ценоза / Н. Б.-о. Бехбудзада, М. В. Минич, И. О. Селиванов и др. // Гавриш. — 2020. — № 3. — С. 42–45.
- Минеральная вата нового поколения - 2. Оценка продуктивности и фенологические наблюдения за растениями гибрида огурца F1 Атлет / Н. Б. Бехбудзада, И. О. Селиванов, М. В. Минич и др. // Гавриш. — 2020. — № 4. — С. 52–55.
- Evangelista-Martínez Z. Isolation and characterization of soil Streptomyces species as potential biological control agents against fungal plant pathogens //World Journal of Microbiology and Biotechnology. – 2014. – Т. 30. – P. 1639-1647.
- Wahyudi A. T. et al. Streptomyces spp. from rhizosphere soil of maize with potential as plant growth promoter //Biodiversitas Journal of Biological Diversity. – 2019. – Т. 20. – №. 9.
- Vos P. et al. (ed.). Bergey's manual of systematic bacteriology: Volume 3: The Firmicutes. – Springer Science & Business Media, 2011. – Т. 3.
- Pacios-Michelena S. et al. Application of Streptomyces antimicrobial compounds for the control of phytopathogens //Frontiers in Sustainable Food Systems. – 2021. – Т. 5. – P. 696518.
- Павлюшин В. А., Новикова И. И., Бойкова И. В. Микробиологическая защита растений в технологиях фитосанитарной оптимизации агроэкосистем: теория и практика (обзор) //Сельскохозяйственная биология. – 2020. – Т. 55. – №. 3. – С. 421-438.
- ГОСТ 12038-84 Семена сельскохозяйственных культур. Методы определения всхожести
- Привалова Н.М., Процай А.А., Литвиненко Ю.Ф., Марченко Л.А., Паньков В.А. Определение фитотоксичности методом проростков // Успехи современного естествознания. – 2006. – № 10. – С. 45-45
- Harir M. et al. Streptomyces secondary metabolites //Basic biology and applications of actinobacteria. – 2018. – Т. 6. – P. 99-122.
- Иркитова А. Н., Каган Я. Р., Соколова Г. Г. Сравнительный анализ методов определения антагонистической активности молочнокислых бактерий //Известия Алтайского государственного университета. – 2012. – №. 3-1. – С. 41-44.
- Джалилов Ф. С. и др. Диагностика зараженности семян томата возбудителем бактериального рака (Clavibacter michiganensis subsp. Michiganensis (Davis (Smith)(Cmm)) методом ПЦР //Известия Тимирязевской сельскохозяйственной академии. – 2007. – №. 1. – С. 21-25.
- Staněk M. et al. Effect of the polysaccharide of Agrobacterium radiobacter on the growth of plants and occurrence of damping-off in sugar beet //Folia Microbiologica. – 1983. – Т. 28. – P. 91-99.
1. Д.Г. Титова*, А.Г. Буланов, О.М. Филатова, Е.Н. Дмитриева, О.Б. Горюнова, Н.С. Марквичев, А.А. Белов Роль экссудатов корневой системы огурца в формировании микробного ценоза при выращивании по малообъемной технологии //Успехи в химии и химической технологии. – 2014. – Т. 28. – №. 5 (154). – С. 70-73.
2. А. А. Шагаев, А. С. Журавлева, Н. Б.-о. Бехбудзада, Марквичев Н.С. и др. Повышение продуктивности растительных экосистем регулированием уровня фитопатогенеза Fusarium oxysporum экссудатами корневой системы растений // Химическая промышленность сегодня. — 2023. — № 2. — С. 7–12. (CAS).
3. Musilova L. et al. Effects of secondary plant metabolites on microbial populations: changes in community structure and metabolic activity in contaminated environments //International journal of molecular sciences. – 2016. – Т. 17. – №. 8. – С. 1205.
4. Минеральная вата нового поколения — формирование микробного ценоза / Н. Б.-о. Бехбудзада, М. В. Минич, И. О. Селиванов и др. // Гавриш. — 2020. — № 3. — С. 42–45.
5. Минеральная вата нового поколения - 2. Оценка продуктивности и фенологические наблюдения за растениями гибрида огурца F1 Атлет / Н. Б. Бехбудзада, И. О. Селиванов, М. В. Минич и др. // Гавриш. — 2020. — № 4. — С. 52–55.
6. Evangelista-Martínez Z. Isolation and characterization of soil Streptomyces species as potential biological control agents against fungal plant pathogens //World Journal of Microbiology and Biotechnology. – 2014. – Т. 30. – P. 1639-1647.
7. Wahyudi A. T. et al. Streptomyces spp. from rhizosphere soil of maize with potential as plant growth promoter //Biodiversitas Journal of Biological Diversity. – 2019. – Т. 20. – №. 9.
8. Vos P. et al. (ed.). Bergey's manual of systematic bacteriology: Volume 3: The Firmicutes. – Springer Science & Business Media, 2011. – Т. 3.
9. Pacios-Michelena S. et al. Application of Streptomyces antimicrobial compounds for the control of phytopathogens //Frontiers in Sustainable Food Systems. – 2021. – Т. 5. – P. 696518.
10. Павлюшин В. А., Новикова И. И., Бойкова И. В. Микробиологическая защита растений в технологиях фитосанитарной оптимизации агроэкосистем: теория и практика (обзор) //Сельскохозяйственная биология. – 2020. – Т. 55. – №. 3. – С. 421-438.
11. ГОСТ 12038-84 Семена сельскохозяйственных культур. Методы определения всхожести.
12. Привалова Н.М., Процай А.А., Литвиненко Ю.Ф., Марченко Л.А., Паньков В.А. Определение фитотоксичности методом проростков // Успехи современного естествознания. – 2006. – № 10. – С. 45-45.
13. Harir M. et al. Streptomyces secondary metabolites //Basic biology and applications of actinobacteria. – 2018. – Т. 6. – P. 99-122.
14. Иркитова А. Н., Каган Я. Р., Соколова Г. Г. Сравнительный анализ методов определения антагонистической активности молочнокислых бактерий //Известия Алтайского государственного университета. – 2012. – №. 3-1. – С. 41-44.
15. Джалилов Ф. С. и др. Диагностика зараженности семян томата возбудителем бактериального рака (Clavibacter michiganensis subsp. Michiganensis (Davis (Smith)(Cmm)) методом ПЦР //Известия Тимирязевской сельскохозяйственной академии. – 2007. – №. 1. – С. 21-25.
16. Staněk M. et al. Effect of the polysaccharide of Agrobacterium radiobacter on the growth of plants and occurrence of damping-off in sugar beet //Folia Microbiologica. – 1983. – Т. 28. – P. 91-99.