Использование Streptomyces для формирования ризосферы в субстрате
19 января 2025, 18:28
журнал «Теплицы России», №2, 2024
В статье проведено исследование различных свойств Streptomyces rimosus B1204 для оценки перспективности использования данного штамма для формирования ризосферы в минераловатном субстрате. Проведена оценка фитотоксичности Streptomyces rimosus B1204 по отношению к огурцам гибрида F1 Атлет и томатам гибрида F1 Сумо. Исследована антагонистическая активность Streptomyces rimosus B1204 по отношению к фитопатогенным бактериям и грибам. Изучена способность Streptomyces rimosus B1204 сохраняться в минераловатном субстрате в присутствии фитопатогенной микрофлоры. Также оценена способность Streptomyces rimosus B1204 к колонизации корневой системы томата. В результате данного исследования показана перспективность применения Streptomyces rimosus B1204 в качестве агента биологического контроля для создания ризосферы при выращивании растений в минераловатном субстрате.
Аннотация
Выращивание культур в защищенном грунте требует высокой квалификаций от агронома. Проблемы физиологии растения, нарушение технологии выращивания, борьба с вредителями и фитопатогенами, соблюдение требований законодательства в области применения пестицидов и агрохимикатов разрешенных к использованию на территории РФ — это минимальный набор задач, которые ежедневно решает агроном защищенного грунта. Несмотря на термин «защищенный грунт» многие параметры в современных теплицах по-прежнему сложно или невозможно контролировать: краткосрочные перебои в энергоснабжении, СО2 для подкормки с фитотоксичными примесями, нехватка рабочего персонала, нарастающий фитопатогенный фон, связанный с бессменным выращиванием культуры и высокой плотностью посадок – в это может приводить к потерям в показателях запланированной урожайности [1]. В ситуации неопределенности важно сосредоточится на параметрах, которые можно успешно скорректировать, а именно по возможности обеспечить культуре соблюдение технологии выращивания и максимально бережную защиту от вредителей и фитопатогенов, которая не приведет к излишнему стрессу и накоплению резистентности у вредных объектов.
Одним из методов современного подхода к защите в условиях тепличного выращивания является применение агентов биологического контроля, в том числе для борьбы против экономически значимых фитопатогенов – Clavibacter michiganensis michiganensis (заболевание бактериальный рак томата), Agrobacterium tumefaciens или Rhisobium radiobacter (заболевание «Бешенство корней», Fusarium oxisporum (заболевание фузариоз), Pythium spp. (корневые и прикорневые гнили), Verticillium spp (заболевание вертциллез) и т.д.
Использование инертных, практически стерильных субстратов на основе минеральной ваты, вермикулита, перлита и др. в тепличном производстве во многом помогло решить проблему с заболеваниями, особенно на начальном этапе выращивания [2]. Но несовершенство методов тестирования семенного материала, разная степень загрязненности источников воды для полива, возврат дренажа и образование биопленки на поверхностях поливной системы в результате длительного оборота выращивания культуры негативно влияют на статистику поражения фитопатогенами. Для создания пролонгированного эффекта от преимуществ, связанных с использованием инертных субстратов, логично было бы формировать безопасный фитостимулирующий биоценоз с самого начала, т.е. с напитки кубиков и матов в рассадном и производственном отделении соответственно.
Первоначальное заселение инертного субстрата микроорганизмами обусловлено процессами обработки и воздушно-капельным переносом. Однако обширное заселение этих сред микроорганизмами, вероятно, происходит только после укоренения растений и прорастания корней в субстрат, за счет выделения растениями органических компонентов - экссудатов, которые служат источниками питания для большинства микроорганизмов [3].
В настоящее время агрономами по защите растений для создания положительного биоценоза активно используются хорошо известные и зарекомендовавшие себя биоагенты – грибы рода Trichoderma spp, бактерии Pseudomonas fluorescence, Bacillus subtilis и Lactobacillus plantarum [4]. Одними из новых и наиболее перспективных, интенсивно изучаемых в качестве агента биологического контроля микроорганизмов, являются бактерии рода Streptomyces. Они представляют важную группу почвенных бактерий из семейства актиномицетов, составляющих от 1 до 20% всех почвенных микроорганизмов [5].
Перспективность Стрептопмицетов
Перспективность Streptomyces spp. в качестве агентов биологического контроля в первую очередь обусловлена их физиологией роста. Образование нитей бактерий рода Streptomyces, которые удлиняются за счет апикального роста и многократно разветвляются, приводит к формированию субстратного мицелия, развивающегося как на поверхности питательной среды, так и внутри неё. Нити мицелия позволяют эффективно использовать питательные вещества, а также позволяют Streptomyces spp. колонизировать различные субстраты и растения [6].
В другую очередь, разнообразие вторичных метаболитов, производимых бактериями рода Streptomyces, представляет огромный потенциал для подавления фитопатогенных грибов и бактерий. При этом продуцируемые вторичные метаболиты, активные в отношении фитопатогенных микроорганизмов, имеют разнообразную природу происхождения, включая антибиотики [7], белки и пептиды [8], летучие органические вещества [9]. Кроме того, их способность метаболизировать различные источники углерода и азота повышает возможность Streptomyces spp. эффективно конкурировать за субстрат при лимите органических компонентов (экссудатов) в ризосфере, при этом взаимодействуя с другими микроорганизмами в градиенте концентраций растительных экссудатов. Не менее важным фактором является способность Streptomyces spp. синтезировать растительные гормоны, относящиеся к классу ауксинов, которые играют важную роль в росте и развитии растений [10].
Таким образом, целью исследования являлась оценка возможности использования бактерий рода Streptomyces для формирования ризосферы в минераловатном субстрате.
Одним из главных свойств агента биологического контроля является отсутствие негативного эффекта на рост и развитие растения. Вследствие этого, на начальном этапе исследования был определен параметр фитотоксичности исследуемого нами штамма - Streptomyces rimosus B1204 (S. rimosus B1204) на семенах огурца и томата.
Для этого проводили глубинное культивирование S. rimosus B1204 в течение 7 суток при температуре 26 ˚С на орбитальном шейкере при 200 об/мин на питательной среде следующего состава (г/л водопроводной воды): маннит - 20; соевая мука - 5; CaCO3 - 3; NH4NO3 - 3. Для оценки фитотоксичности чашку Петри с 2 слоями стерильной фильтровальной бумаги (марка Ф) увлажняли 3 мл стерильной воды (контроль) или 3 мл, разбавленной в 100 раз культуральной жидкости исследуемого штамма. В полученные влажные камеры выкладывали семена огурца гибрида F1 Атлет или семена томата гибрида F1 Сумо. Все варианты исследовали в нескольких проворностях. Проращивали семена в течение 7 суток в одинаковых условиях в термостате при температуре 28 ˚С, без освещения. На 3 сутки определяли энергию прорастания семян, на 7 сутки - всхожесть согласно ГОСТ [11]. Также на 7 сутки определяли среднюю длину вегетативной части проростков и среднюю массу проростков.
После измерения всех параметров оценивали фитотоксичный эффект [12] по формуле:
где Мк – средняя масса проростков в контрольной пробе, Моп – средняя масса проростков в опытной пробе.
В случае, если показатель фитотоксичности был больше 15%, образец считался токсичным для растений, если менее -15%, то фитостимулирующим. В случае, если фитотоксичный эффект попадал в интервал от -15% до 15%, эффект образца считался нейтральным. Результаты представлены в таблицах 1-2.
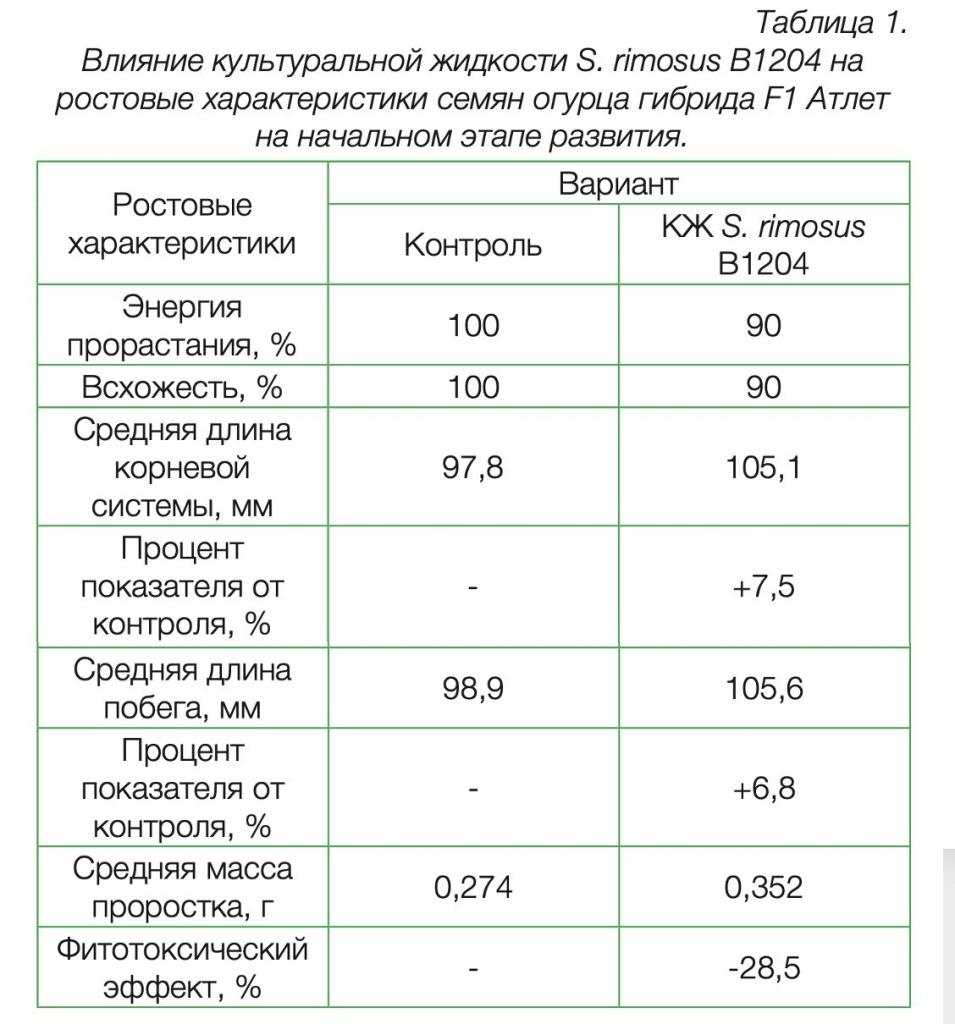

В результате исследования было показано, что штамм S. rimosus B1204 не оказывает негативное влияние на рост и развитие семян огурца гибрида F1 и томата F1, более того культуральная жидкость S. rimosus B1204 оказывает фитостимулирующее действие, что подтверждается увеличением средней массы проростков и развитой корневой системой.
Способность рода Streptomyces к синтезу активных метаболитов, способных подавлять рост фитопатогенной микрофлоры, – как грибной, так и бактериальной – является важным свойством при выборе микроорганизма для применения в составе биологических средств для защиты растений. Таким образом, вторым этапом исследования являлась оценка антагонистической активности штамма S. rimosus B1204 по отношению к фитопатогенным микроорганизмам.
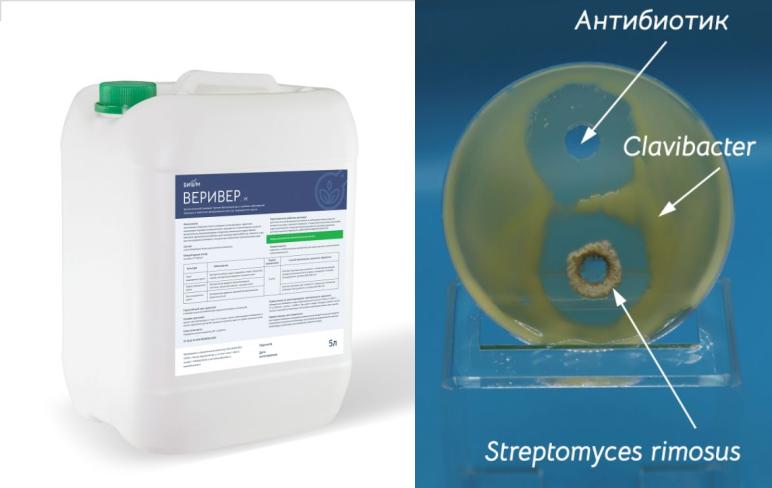
Взаимодействие штамма S. rimosus B1204 и фитопатогенных бактериальных культур оценивали по стандартной методике – методу «лунок» [13]. Для этого поверхность агаризованной питательной среды с заранее вырезанными лунками засевали газоном тест-объектами. В качестве тест-объектов были выбраны бактерии Clavibacter michiganensis subsp. michiganensis (C. michiganensis), вызывающий бактериальное увядание и рак томата, а также Rhizobium radiobacter (устар. Agrobacterium tumefaciens) (R. radiobacter), вызывающий неконтролируемое развитие корневой системы и образование опухолевых образований у растительных культур, именуемых корончатыми галлами. В лунки помещали культуральную жидкость S. rimosus B1204 объемом 200 мкл, в контрольные лунки помещали раствор антибиотика объемом 200 мкл в концентрации 0,5 г/л. Далее чашки Петри помещали в термостат для инкубации при температуре 26 ˚С в течение 24 часов. Антагонистическую активность оценивали по радиусу зоны задержки роста тест-объектов.
Результаты представлены на рисунке 1.
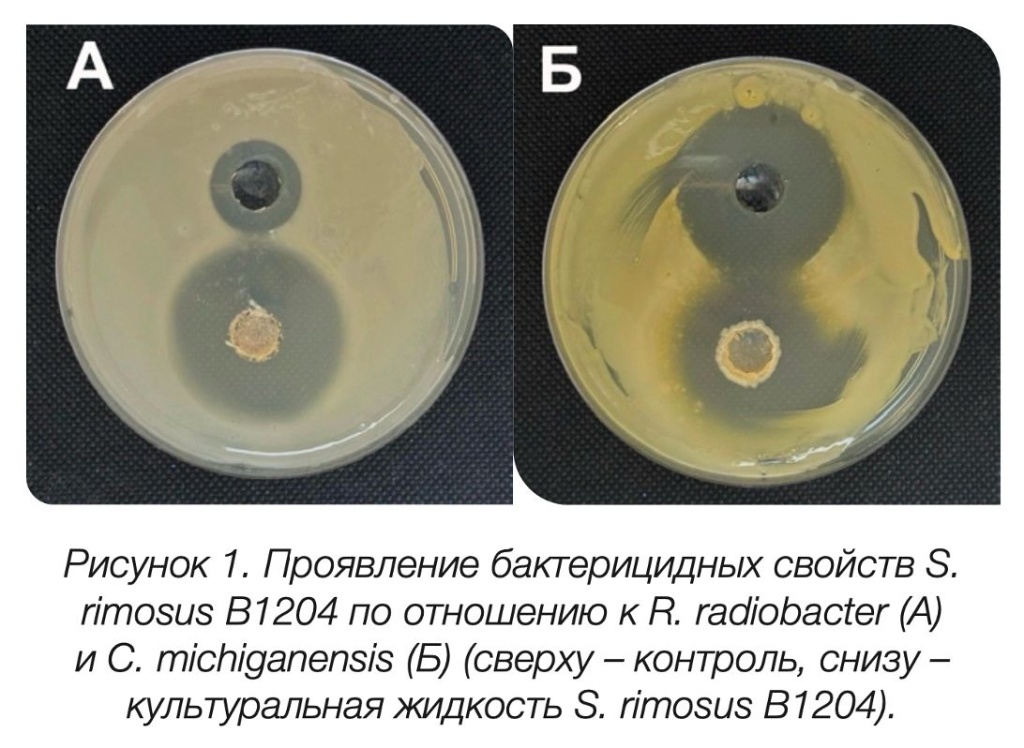
Из представленных на рисунке 1 результатов можно заметить, что зона задержки роста наблюдается во всех случаях рассматриваемых бактериальных фитопатогенов, при этом радиус задержки роста штаммом S. rimosus B1204 соизмерим, в случае C. michiganensis, или больше, в случае R. radiobacter, по размеру с радиусом задержки роста в контрольном варианте. Таким образом, можно сделать вывод, что S. rimosus B1204, проявляя антагонистическую активность, подавляет рост фитопатогенных бактериальных культур C. michiganensis и R. radiobacter
Для оценки фунгицидных свойств штамма S. rimosus B1204 на поверхность агаризованной среды Чапека в центр уколом подсевали тест-объекты – Fusarium sp., Cylindrocarpon sp. и Alternaria sp., затем, отступая 2,5 см от центра, микробиологической иглой наносили штрихом биомассу S. rimosus B1204. В качестве контроля выступала сторона чашки без штриха. Далее чашки Петри помещали в термостат для инкубации при температуре 26 ˚С в течение 72 часов. По окончании инкубации сравнивали радиус грибной колонии на контрольной стороне и на стороне со штрихом S. rimosus B1204.
Результаты представлены на рисунке 2.
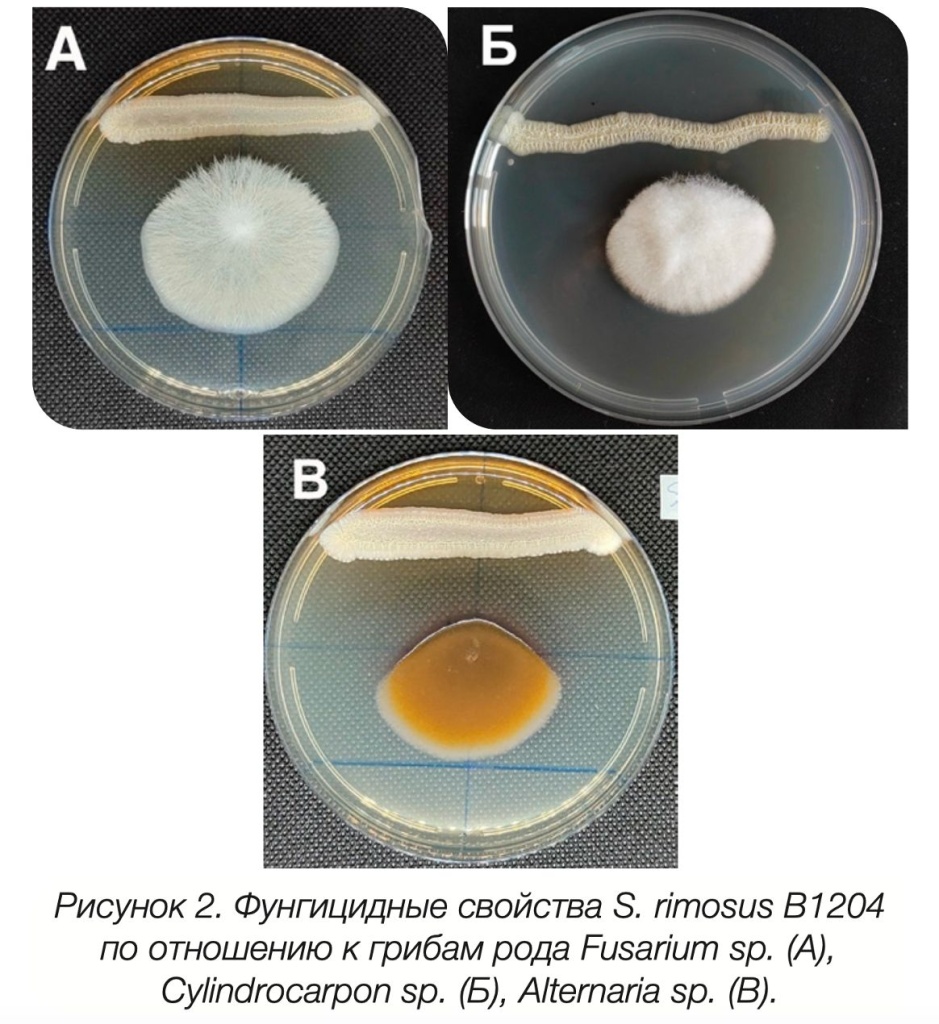
Из рисунка 2 видно, что рост фитопатогенных грибов преимущественно направлен в сторону, противоположную колониям S. rimosus B1204, то есть в зону более благоприятную для жизнедеятельности, что может быть связано с производством штаммом S. rimosus B1204 активных вторичных метаболитов или с его способностью конкурировать за субстрат при поверхностном росте. Результаты свидетельствуют о том, что S. rimosus B1204 проявляет фунгицидные свойства по отношению к фитопатогенным грибам Fusarium sp., Cylindrocarpon sp. и Alternaria sp.
Таким образом, показано, что S. rimosus B1204 способен синтезировать вторичные метаболиты бактерицидной и фунгицидной природы, активные против фитопатогенных микроорганизмов. В следующем этапе было исследовано взаимодействие S. rimosus B1204 и фитопатогенной микрофлоры непосредственно в минераловатном субстрате. При этом оценивалась способность исследуемого штамма сохраняться в инертном субстрате с растением томата при высоких концентрациях бактериального фитопатогена – R. radiobacter.
Для проведения исследования в стерильный минераловатный субстрат вносили семена томата гибрида F1 Сумо, присыпая его 1 г вермикулита и напитывая стерильным раствором солей Хогланда в объеме 500 мл. В минераловатный субстрат вносили культуральные жидкости микроорганизмов S. rimosus B1204 до концентрации 1*107 и R. radiobacter до концентрации 1*107. В качестве контроля выступал субстрат, в который вместе с посевом семян вносили культуральную жидкость только R. radiobacter до концентрации 1*107. В течение 28 суток оценивали концентрацию микроорганизмов в субстрате. Для этого отбирали 1 г минераловатного субстрата и смывали клетки микроорганизмов в стерильном физиологическом растворе объемом 9 мл. Далее с помощью метода последовательных разведений Коха [14] определяли концентрацию S. rimosus B1204 и R. radiobacter.
Результаты представлены на рисунке 3.
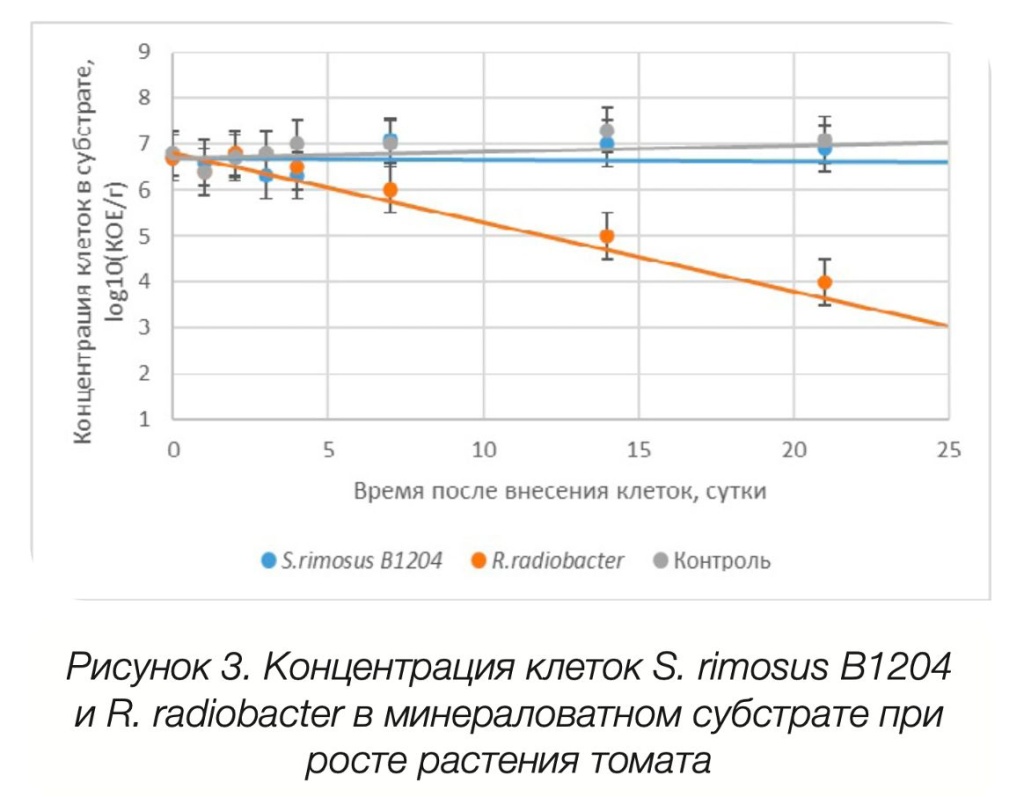
Из результатов исследования видно, что при совместном внесении в минераловатный субстрат на начальных этапах развития томата S. rimosus B1204 и бактериального фитопатогена - R. radiobacter концентрация последнего снижалась, чего не наблюдалось в контрольном варианте. В свою очередь концентрация S. rimosus B1204 сохранялась на протяжении не менее 22 суток. Таким образом, можно сделать вывод, что S. rimosus B1204 способен развиваться в присутствии фитопатогенного микроорганизма - R. radiobacter в минераловатном субстрате.
Также была оценена способность S. rimosus B1204 колонизировать корневую систему томата на начальных этапах развития растения, выращенного в присутствии исследуемого штамма, что является очень важным свойством агента биологического контроля.
Результат представлен на рисунке 4.
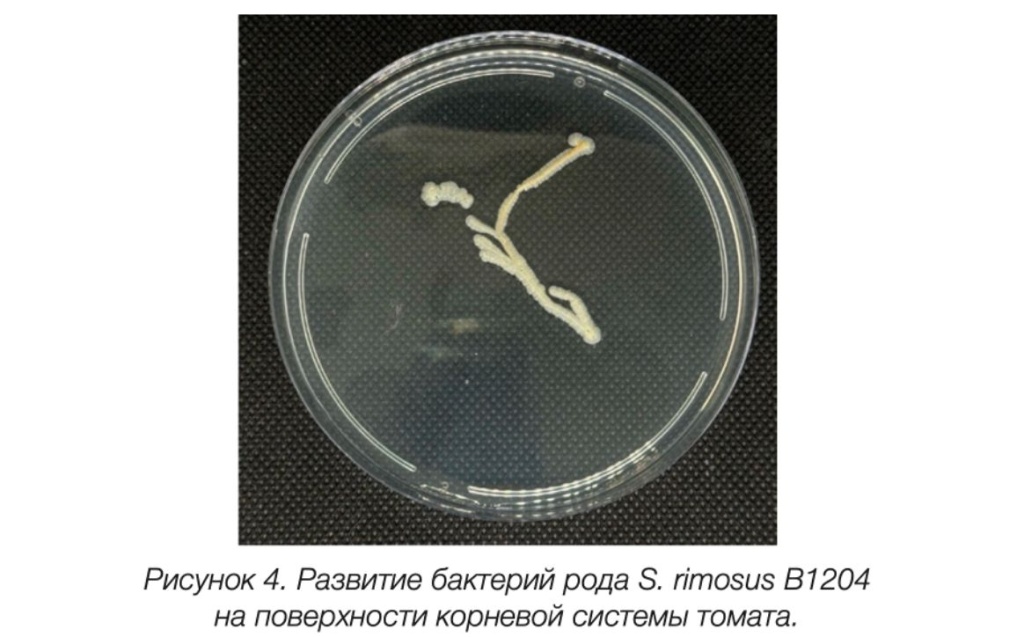
Из рисунка 4 видно, что корневая система томата полностью покрыта клетками S. rimosus B1204, отсюда можно сделать вывод, что исследуемый штамм хорошо колонизирует корневую систему томата, что может давать конкурентное преимущество данному штамму перед фитопатогенной микрофлорой.
Таким образом, Streptomyces rimosus B1204 благодаря своим свойствам является перспективным микроорганизмом для создания препарата, предназначенного для биологической защиты растений. Именно поэтому данный штамм был выбран в качестве основы для разработки препарата ВЕРИВЕР, Ж (ГК БИОМ), который может быть использован как на этапе формирования микробного сообщества в прикорневой зоне растений, так и на последующих этапах для корректировки его состава и регулирования численности грибных и бактериальных фитопатогенов.
Список литературы
- Скульская Л.В., Широкова Т.К. Проблемы и перспективы овощеводства закрытого грунта // Norwegian Journal of Development of the International Science. - 2020. - №39. - С. 35-39.
- Carlile W.R., Wilson D.P. Microbial Activity in Growing Media - A Brief Review // Acta Horticulture. - 1991. - №294. - С. 197-206.
- Д.Г. Титова*, А.Г. Буланов, О.М. Филатова, Е.Н. Дмитриева, О.Б. Горюнова, Н.С. Марквичев, А.А. Белов. Роль экссудатов корневой системы огурца в формировании микробного ценоза при выращивании по малообъемной технологии //Успехи в химии и химической технологии. – 2014. – Т. 28. – No. 5 (154). – С. 70-73.
- Штерншис М. В. Биологическая защита растений / М. В. Штерншис, И. В. Андреева, О. Г. Томилова. – 2-е, Исправленное, Дополненное. – Санкт-Петербург: Издательство Лань, 2018. – 332 с.
- El-Tarabily K., Alkhajeh A. Field performance of endophytic actinomy- cetes in relation to plant growth promotion and biological control of Fusarium oxysporum a pathogen of tomato. // American Phytopathological Society. - USA: 2016. - С. 55-55.
- Oluwaseyi Samuel Olanrewaju, Olubukola Oluranti Babalola. Streptomyces: implications and interactions in plant growth promotion // Applied Microbiology and Biotechnology. - 2019. - №103. - С. 1179–1188.
- Jeong Do Kim, Jae Woo Han, Sung Chul Lee, Dongho Lee, In Cheon Hwang, Beom Seok Kim. Disease control effect of strevertenes produced by Streptomyces psammoticus against tomato Fusarium wilt // Journal of agricultural and food chemistry. - 1893-1899, 2011. - №59 (5).
- Jones S., Pham C., McKillip J., Zambri M., Carlson E. and Elliot M. Streptomyces volatile compounds influence exploration and microbial community dynamics by altering iron availability. // BioRxiv. – 2018.
- Fernanda J., Calderón-de la Sancha, Ulises Carrasco-Navarro, Gerardo Santander, Javier Barrios-González, Armando Mejía Novel. Antimicrobial activity of protein produced by Streptomyces lividans TK24 against the phytopathogen Clavibacter michiganensis // Archives of Microbiology. - 2022. - №204.
- Manulis S., Shafrir H., Epstein E., Lichter A. & Barash I. Biosynthesis of indole-3-acetic acid via the indole-3-acetamide pathway in Streptomyces spp. // Microbiology. - 2010. - №140. - С. 1045–1050.
- ГОСТ 12038-84 Семена сельскохозяйственных культур. Методы определения всхожести.
- Привалова Н.М., Процай А.А., Литвиненко Ю.Ф., Марченко Л.А., Паньков В.А. Определение фитотоксичности методом проростков // Успехи современного естествознания. – 2006. – No 10. – С. 45–45.
- Иркитова А.Н., Каган Я.Р., Соколова Г.Г. Сравнительный анализ методов определения антагонистической активности молочнокислых бактерий // Известия Алтайского государственного университета. – 2012. – No. 3-1. – С. 41–44.
- Лабораторный практикум по общей микробиологии / Н.Б. Градова и др.- М.: ДеЛи принт. 2001. С. 131.
1. Скульская Л.В., Широкова Т.К. Проблемы и перспективы овощеводства закрытого грунта // Norwegian Journal of Development of the International Science. - 2020. - №39. - С. 35-39.
2. Carlile W.R., Wilson D.P. Microbial Activity in Growing Media - A Brief Review // Acta Horticulture. - 1991. - №294. - С. 197-206.
3. Д.Г. Титова*, А.Г. Буланов, О.М. Филатова, Е.Н. Дмитриева, О.Б. Горюнова, Н.С. Марквичев, А.А. Белов. Роль экссудатов корневой системы огурца в формировании микробного ценоза при выращивании по малообъемной технологии //Успехи в химии и химической технологии. – 2014. – Т. 28. – No. 5 (154). – С. 70-73.
4. Штерншис М. В. Биологическая защита растений / М. В. Штерншис, И. В. Андреева, О. Г. Томилова. – 2-е, Исправленное, Дополненное. – Санкт-Петербург: Издательство Лань, 2018. – 332 с.
5. El-Tarabily K., Alkhajeh A. Field performance of endophytic actinomy- cetes in relation to plant growth promotion and biological control of Fusarium oxysporum a pathogen of tomato. // American Phytopathological Society. - USA: 2016. - С. 55-55.
6. Oluwaseyi Samuel Olanrewaju, Olubukola Oluranti Babalola. Streptomyces: implications and interactions in plant growth promotion // Applied Microbiology and Biotechnology. - 2019. - №103. - С. 1179–1188.
7. Jeong Do Kim, Jae Woo Han, Sung Chul Lee, Dongho Lee, In Cheon Hwang, Beom Seok Kim. Disease control effect of strevertenes produced by Streptomyces psammoticus against tomato Fusarium wilt // Journal of agricultural and food chemistry. - 1893-1899, 2011. - №59 (5).
8. Jones S., Pham C., McKillip J., Zambri M., Carlson E. and Elliot M. Streptomyces volatile compounds influence exploration and microbial community dynamics by altering iron availability. // BioRxiv. – 2018.
9. Fernanda J., Calderón-de la Sancha, Ulises Carrasco-Navarro, Gerardo Santander, Javier Barrios-González, Armando Mejía Novel. Antimicrobial activity of protein produced by Streptomyces lividans TK24 against the phytopathogen Clavibacter michiganensis // Archives of Microbiology. - 2022. - №204.
10. Manulis S., Shafrir H., Epstein E., Lichter A. & Barash I. Biosynthesis of indole-3-acetic acid via the indole-3-acetamide pathway in Streptomyces spp. // Microbiology. - 2010. - №140. - С. 1045–1050.
11. ГОСТ 12038-84 Семена сельскохозяйственных культур. Методы определения всхожести.
12. Привалова Н.М., Процай А.А., Литвиненко Ю.Ф., Марченко Л.А., Паньков В.А. Определение фитотоксичности методом проростков // Успехи современного естествознания. – 2006. – No 10. – С. 45–45.
13. Иркитова А.Н., Каган Я.Р., Соколова Г.Г. Сравнительный анализ методов определения антагонистической активности молочнокислых бактерий // Известия Алтайского государственного университета. – 2012. – No. 3-1. – С. 41–44.
14. Лабораторный практикум по общей микробиологии / Н.Б. Градова и др.- М.: ДеЛи принт. 2001. С. 131.